В настоящее время Периодический закон Д. И. Менделеева имеет следующую формулировку:
| Свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений, находятся в периодической зависимости от величины зарядов ядер их атомов. |
Свойства, изменяющиеся периодически и встречающиеся на ЕГЭ: окислительные и неметаллические, восстановительные и металлические, радиус атома, заряд ядра, электроотрицательность.
- Металлические (восстановительные) свойства – способность атомов отдавать электроны.
- Неметаллические (окислительные) свойства – способность атомов присоединять электроны.
- Электроотрицательность (ЭО) – способность атомов притягивать валентные электроны других атомов. Она изменяется вместе с неметаллическими свойствами: возрастает слева направо и снизу вверх.
- Основные свойства – это совокупность свойств, проявляемых основаниями, главное - способность реагировать с кислотами, а также кислотными оксидами.
- Кислотные свойства – это совокупность свойств, проявляемых кислотами, главные – отдавать протоны и принимать электроны, реагировать с основаниями и основными оксидами.

Условное деление таблицы надвое
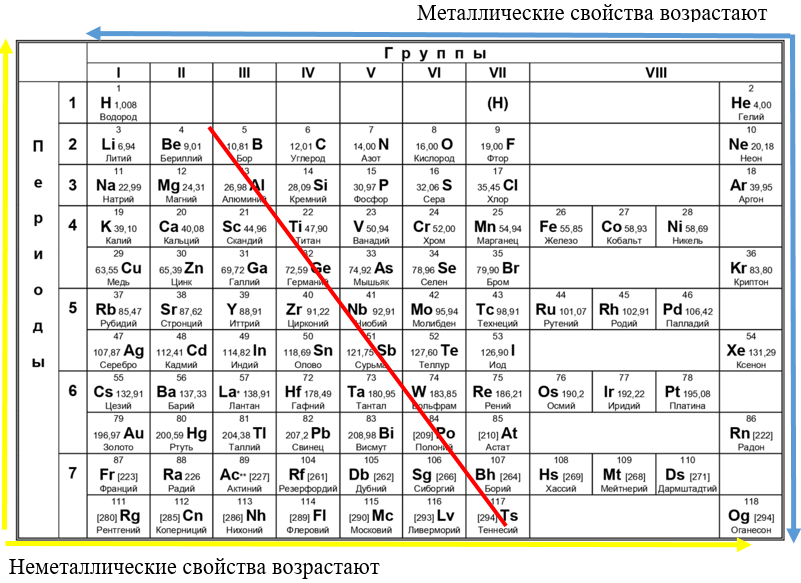
Примерно так делят таблицу Менделеева, сверху справа остаются неметаллы, снизу слева – металлы, опять же актуально только для главных подгрупп. Жёлтыми стрелками на рисунке показано в каких направлениях возрастают неметаллические (окислительные) свойства: слева направо по периодам и снизу вверх по главным подгруппам. Голубыми же – направления возрастания металлических (восстановительных) свойств: справа налево по периодам и сверху вниз по главным подгруппам. Соответственно, когда металлические свойства возрастают, ослабевают кислотные и наоборот.
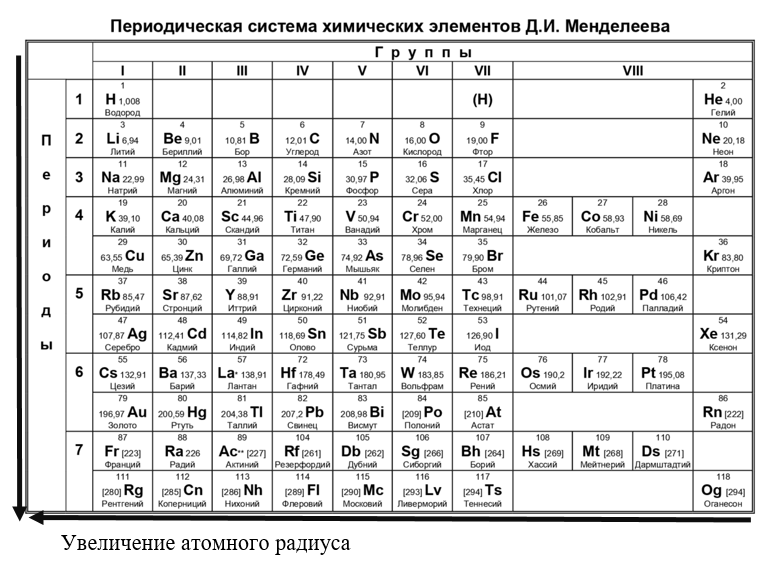
Заряд ядра, радиус атома
Заряд ядра равен номеру элемента, так как отражает количество протонов, поэтому в периодах слева направо и в группах сверху вниз он будет увеличиваться. Зато атомный радиус не так прост: в периодах слева направо он будет уменьшаться из-за большего притяжения электронов к ядру, а в группах - увеличиваться, так как внешние электроны будут располагаться дальше от ядра. На рисунке это показано чёрными стрелками:
Свойства высших оксидов, гидроксидов и летучих водородных соединений.
Основные и неметаллические свойства высших оксидов и гидроксидов будут меняться так же как металлические и неметаллические свойства соответствующих элементов: с ростом металлических свойств элементов растут и основные свойства их высших оксидов и гидроксидов, а сростом неметаллических растут кислотные свойства. Но кислотность летучих водородных соединений изменяется не совсем так: как и кислотные свойства высших оксидов и гидроксидов она увеличивается в периодах слева направо, а вот в группах наоборот – она увеличивается сверху вниз, образовывать их могут только неметаллы IVA-VIIA подгрупп.
Тест по теме “Периодический закон”
Разбор:
Набранные баллы:
5
Смотреть разбор
Отправить тест на проверку?
Ты решил еще не все задания












