Оксиды – интересные и уникальные вещества. Они очень распространены в окружающей среде: стекло (основной компонент ), алюминиевая посуда (снаружи покрыта прочной оксидной пленкой
), ржавчина на железе (
), песок на пляже (опять же
), газированные напитки (
)... Причина их широкой распространенности – хорошая реакционная способность кислорода воздуха окислять практически всё на своём пути. По этой же причине так мало металлов и неметаллов, которые в природе находятся в самородном состоянии.
Что такое оксид
Оксид – это бинарное соединение, содержащее кислород со степенью окисления -2. Важно помнить, что к оксидам не относятся пероксиды и надпероксиды. Пероксид – бинарное соединение, содержащее кислород со степенью окисления -1. Например, или
. Надпероксид (или супероксид) – бинарное соединение, содержащее кислород со степенью окисления -1/2. Например,
.
Классификация оксидов
А теперь рассмотрим классификацию оксидов:
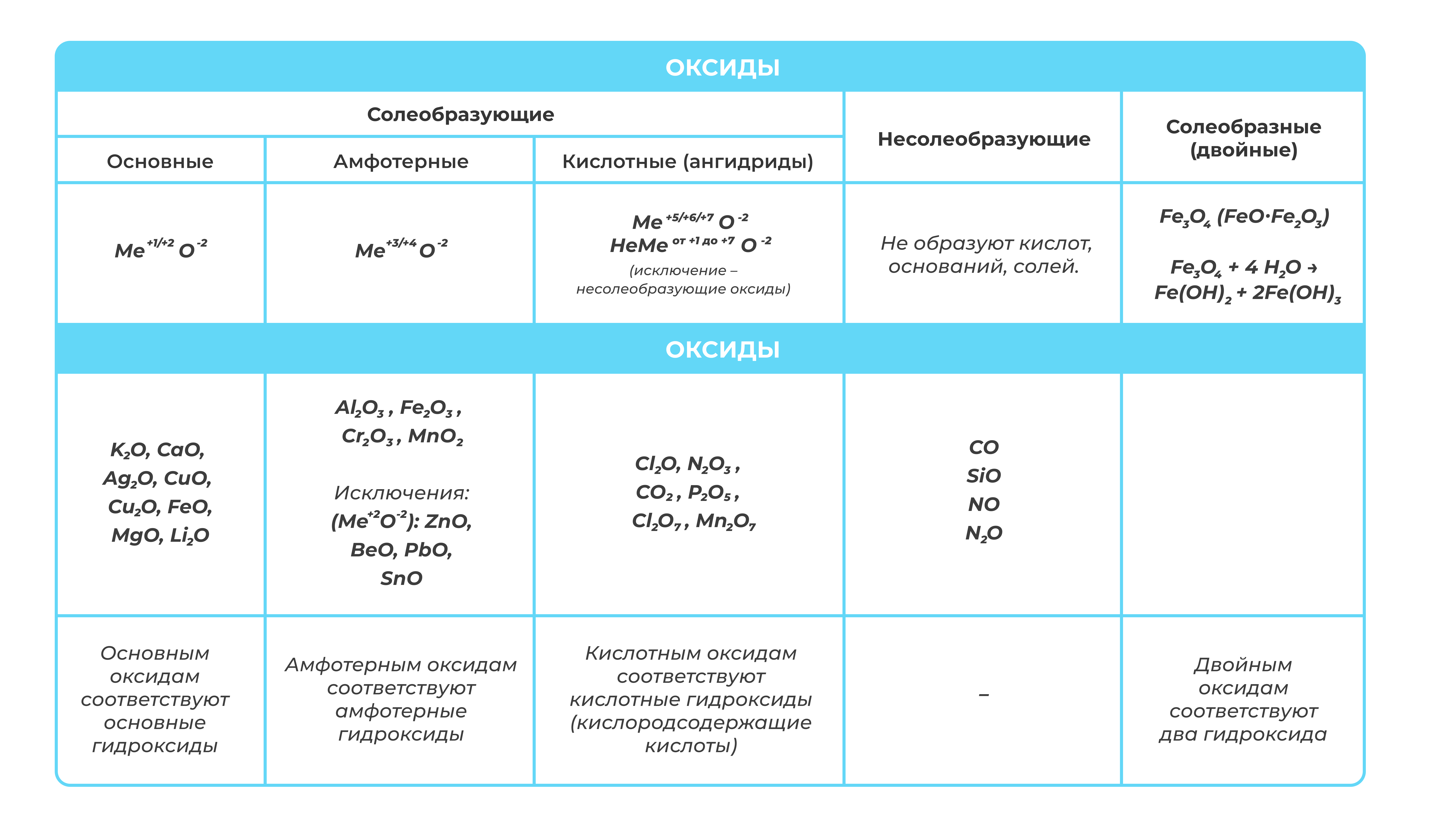
Физические свойства оксидов
Оксиды встречаются во всех трёх агрегатных состояниях, которое зависит от вида оксида.
- Кислотные и несолеобразующие оксиды.
Газообразное состояние встречается только у оксидов неметаллов: углекислого газа – , бурого газа –
, сернистого газа –
, веселящего газа –
и угарного газа
. В жидком состоянии встречаются
(зеленовато-бурый или красный маслянистый),
(бесцветный) и
(синий)...
Оксиды неметаллов встречаются и в твёрдом агрегатном состоянии. Они имеют молекулярную кристаллическую решетку и низкие температуры плавления (искл. – атомная КР и высокая
).

- Основные и амфотерные оксиды.
Такие оксиды при обычных условиях – твердые вещества, которые имеют ионную кристаллическую решетку и высокие температуры плавления.

В природе существуют примеры оксидов, которые разлагаются при высокой температуре. Например, оксид ртути(II) распадается на простые вещества при 500°C :
Такой способ получения кислорода в 1774 году открыл английский ученый Джозеф Пристли.
Задания
А теперь попробуем разобрать на примерах, где нам эти знания пригодятся на ЕГЭ.
1. Составь формулу оксида элемента в высшей степени окисления, расположенного в:
а. VA группе 3 периода;
б. IIIA группе 3 периода;
в. VIIA группе 3 периода;
г. IIB группе 4 периода.
Укажи его характер.
Ответ: – кислотный оксид,
– амфотерный оксид,
– кислотный оксид,
– амфотерный оксид.
2. Среди предложенных формул веществ, расположенных в пронумерованных ячейках, выбери формулы: А) амфотерного оксида; Б) кислотного оксида; В) несолеобразующего оксида.
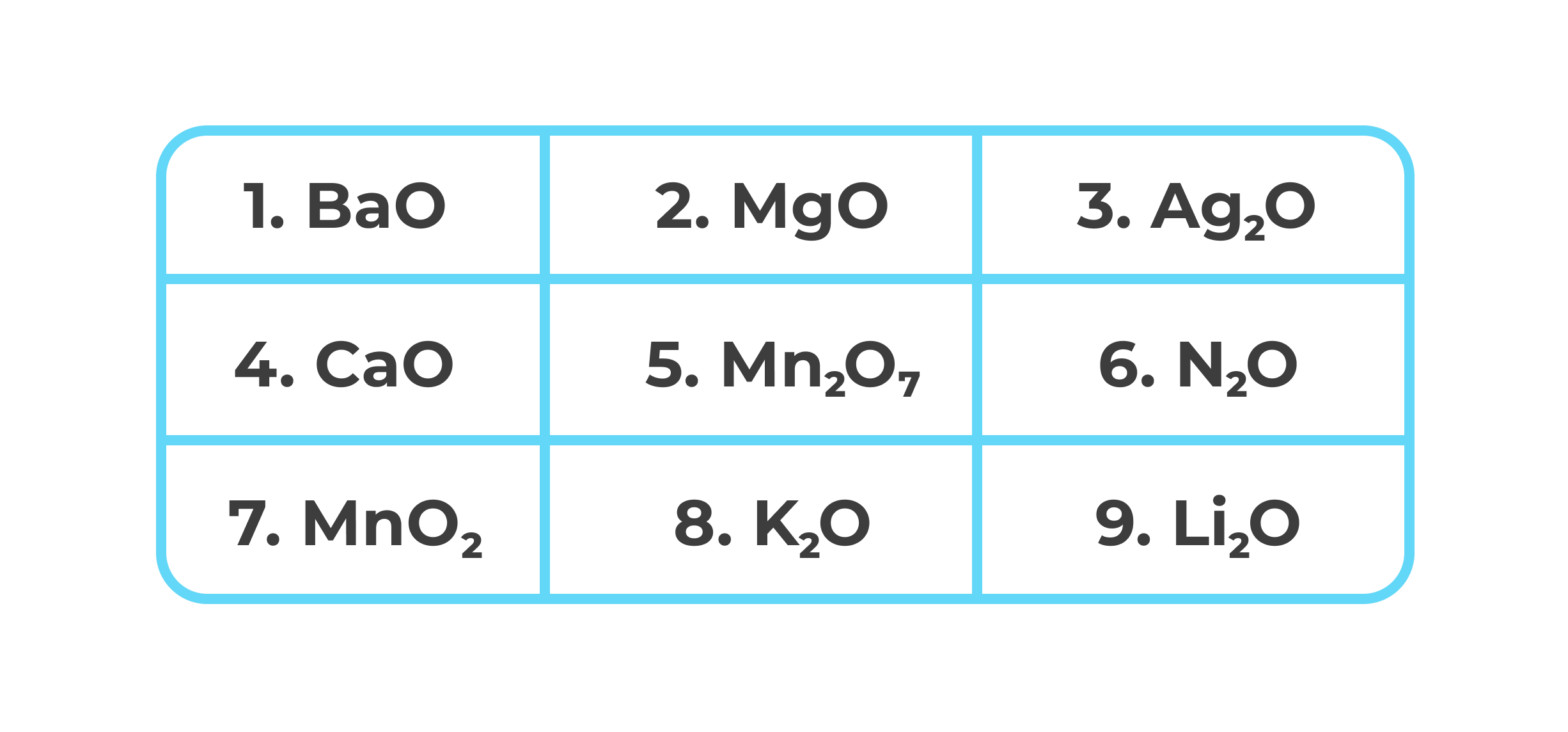
Ответ: 756











